A tengervíz kemizmusa
Tudomány1/2. oldal
A tenger enciklopédiájának újabb fejezete abban segít, hogy magának a tengernek a vizét jobban megismerhessük.
A tengervíz sótartalma
 |
|
Albumhoz klikk a képre.
|
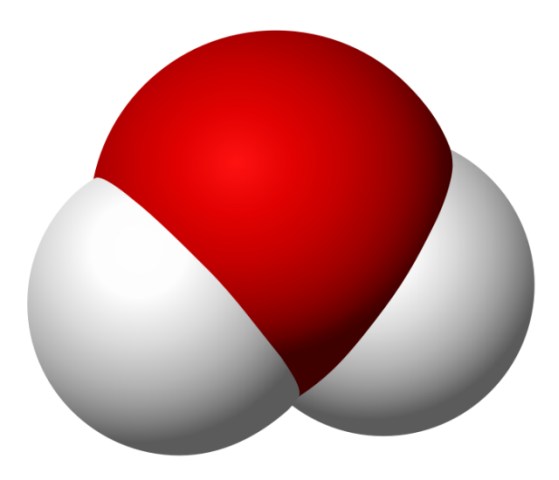
A vízmolekulán belül az oxigén és a hidrogénatomok kötésének a módja az, ami meghatározza a víz egyedi tulajdonságait. A vízmolekulát alkotó atomok ugyanis aszimmetrikus kötésűek. A vízmolekula V formára emlékeztető szerkezetén belül, a csúcsok enyhén negatív, illetve pozitív töltésűek. Az ellentétes elektromos töltéssel rendelkező részecskék között alakul ki az ún. ionos kötés, amelynek az a lényege, hogy mindig az ellentétes töltésű részecskék között jön létre a kapcsolódás. A tengervízben oldott ásványi anyagok közül a nátrium (Na) és a klór (Cl) együttes aránya kb. 85%. A pozitív töltésű nátriumionok és a negatív töltésű klórionok összekapcsolódásával jön létre a rácsos kristályszerkezetű konyhasó. A vízmolekulák képesek viszonylag gyorsan behatolni a kristályos szerkezetű konyhasót tartalmazó vegyületekbe, ahol a hidrogén a klórhoz, az oxigén pedig a nátriumhoz kapcsolódik, kiszakítva, kioldva ezeket az elemeket. Kémiailag a vízmolekula ellentétes polaritása eredményezi azt, hogy a víz a leghatékonyabb természetes oldószer.
Az óceánok kialakulásáról írt fejezetünkben már bemutattuk, hogy a Föld hidroszférája a felszíni olvadt kőzetek lehűlésével egyidejűleg, az ún. kigázosodás során jött létre. A megszilárduló földkéregből az őslégkörbe került hatalmas mennyiségű vízgőz kicsapódásakor, vízzel töltődtek fel a kéreg egyenetlenségei. A lehulló, és az alacsonyabban fekvő medenceterületeket kitöltő víz azonban még édesvíz volt. A kigázosodási folyamat azonban nem csak vízgőzt, hanem más gázokat, így többek között rendkívül nagy mennyiségű szén-dioxidot (CO2) is a légkörbe juttatott. Az őslégkörben felhalmozódott széndioxid az esőcseppekbe oldódva, a heves esőzésekkel került be a kialakuló hidroszférába. Emiatt az édesvizek kémhatása savassá vált. A savas víz pedig még a tiszta víznél is hatékonyabb oldószer. A vízkörzés hatására, hosszú százmillió évek alatt, a szilárd kéreget alkotó szinte valamennyi elemből álló oldattá alakult át az ősóceánok vize. A tengervízből, igaz, hogy csak rendkívül alacsony mennyiségben és eltérő arányban, de a periódusos rendszer szinte valamennyi elemét kimutathatjuk. A tengervízben oldott anyagok között hét komponens a meghatározó. A kloridok (Cl) 55%, a nátrium (Na) 30,6%, a szulfátok (SO2) 7,7%, a magnézium (Mg2) 3,7%, a kalcium (Ca2) 1,2%, a kálium (K) 1%, míg a bikarbonátok (HCO2) 0,4% arányban alkotják a "tengeri sót". A tengervíz sótartalmát a vízben oldott ásványi anyagok fajlagos mennyisége fejezi ki. Ezt a mennyiséget súlyezrelékben határozzuk meg. A súlyezrelék az egy kilogramm tömegű (egy liter térfogatú) tengervízben mért oldott ásványi anyagok tömege, grammban meghatározva.
A világtenger szalinitása stabilnak tekinthető. A nyílt vizek sótartalma egységesen és átlagosan 34,5-35 súlyezrelék. A zártabb medencék sóháztartása ettől eltérő értékeket mutathat a párolgás intenzitásának, a vízutánpótlás mértékének, az éghajlati tényezők, és a beömlő édesvíz mennyiségének a függvényében. A világtenger standard szalinitási értékénél magasabb sótartalmú vizeket túlsós, szuperhalin vizeknek, az ennél alacsonyabb sótartalmú vizeket pedig csökkentsós, vagy brakkvizeknek nevezzük. A szalinitás értéke döntő hatást gyakorol a tengeri élővilág biodiverzitására. A tengeri élőlények jelentős többsége a sótartalom változására érzékeny, ún. stenohalin szervezet, és csupán marginális kissebségük tekinthető a sótartalom változását (különösen a sótartalom csökkenését) toleráló, euryhalin szervezetnek. Az őslénytani leletek azt bizonyítják, hogy legalább 350 millió éve változatlan a világtenger kemizmusa. Valószínű, hogy a stabil sóháztartás ennél már sokkal korábban kialakult, de az ezt egyértelműen bizonyító fosszilis anyag még meglehetősen hiányos.
Az írás a következő lapon folytatódik!
 (átlag: 3.8) átlagos nehézségű
(átlag: 3.8) átlagos nehézségű 





 Thaiföld
Thaiföld
